Enfermedad de Chagas: una infección sistémica de difícil tratamiento

A más de 100 años del descubrimiento de la enfermedad de Chagas también llamada tripanosomiasis americana- ésta continúa siendo un gran desafío en cuanto a su diagnóstico y tratamiento, pues no siempre resulta efectivo o accesible para los afectados.
Esta enfermedad consiste en una infección sistémica de elevada prevalencia en Latinoamérica, de difícil tratamiento y graves complicaciones, pues afecta principalmente a órganos claves como el corazón, el intestino grueso y el esófago.
El incremento de las rutas comerciales de los actuales países emergentes, sumado a la modernización y mayor alcance de los medios de transporte, ha hecho más difícil controlar esta enfermedad, por lo que la globalización ha jugado un papel fundamental en su distribución a nivel mundial.
Vías de transmisión
La enfermedad de Chagas es producida por el protozoo Trypanosoma cruzi (T.cruzi), que se transmite de cinco formas:
- Transmisión vectorial: que es la más común, desde numerosos reservorios animales (domésticos y selváticos), principalmente a través de un insecto vector conocido genéricamente como triatominos -con diferentes denominaciones en los países- como la vinchuca en Argentina y Chile, o la chinche besucona en México.
Más de 150 especies de triatóminos son portadores del T. cruzi. Estos insectos succionan la sangre de las personas, y después de picar, defecan en la herida, facilitando que el parásito se introduzca en el organismo y se extienda a través del torrente circulatorio.
- Vía congénita o vertical, es decir, de madres a hijos, que representa un gran riesgo, dado que la mayor parte de las embarazadas con enfermedad de Chagas están en la fase crónica de la enfermedad y suelen ser asintomáticas, pero presentan mayor riesgo de parto pretérmino, recién nacido con bajo peso al nacer e incluso muerte fetal.
- Transfusiones de hemoderivados y de trasplante de tejidos no testeados, en países que no se analizan las muestras de sangre de los donantes.
- Por vía oral, a través de la ingesta de zumos de caña de azúcar, açaí o guayaba contaminados con el parásito. Se da solo en países donde existe el insecto vector.
- Accidentes de laboratorio, si bien es muy poco frecuente, se puede contraer por pinchazos o exposición de mucosas, por parte de profesionales que manipulan muestras que contienen el parásito o que trabajan directamente con el insecto vector.
Perfil epidemiológico
Hay personas infectadas por T.cruzi en los 21 países de América Latina, de los cuales dos terceras partes pertenecen al Cono Sur. Los países con más casos son Argentina, Brasil y México, seguido de Bolivia.
Los incesantes flujos migratorios han favorecido la llegada de personas con esta enfermedad a regiones anteriormente consideradas no endémicas, como eran Estados Unidos, Europa, Asia y Oceanía.
La Organización Mundial de la Salud estima que la cifra de infectados en México asciende a 1,1 millones, que además se ubica en los primeros lugares en transmisión vectorial, pues existen 13 transmisores de importancia para el humano, tanto dentro del hogar como fuera de él, seguido por transmisión debida a transfusión sanguínea.
Clínica: indicios de la enfermedad y su diagnóstico
La enfermedad de Chagas se divide en fase aguda y fase crónica:
En la fase aguda, los síntomas se inician entre 7 y 10 días tras la infección por T.cruzi, y consiste, habitualmente en manifestaciones leves e inespecíficos que habitualmente pasan inadvertidas, pues son parecidas a un cuadro gripal, como fiebre, malestar general, hepatoesplenomegalia (aumento del tamaño del hígado).
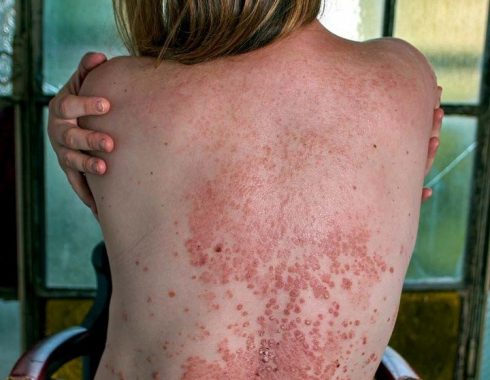
Ocasionalmente pueden aparecer lesiones cutáneas que indican el lugar de la inoculación, como nódulos cutáneos (chagoma de inoculación) o un edema y conjuntivitis que involucra un solo ojo, denominado signo de Romaña.
La fase crónica se inicia aproximadamente 1-2 meses después de la infección, donde los pacientes están asintomáticos, sin embargo, un porcentaje de ellos desarrolla complicaciones varias décadas post infección, con predominio de problemas cardíacos, digestivos o mixtos.
Se calcula que alrededor del 40 al 60% de los pacientes con enfermedad de Chagas desarrollarán cardiopatía chagásica, que predispone a la formación de coágulos y donde el principal indicio de esta patología son los trastornos electrocardiográficos, que pueden terminar en la muerte súbita del paciente.
A nivel gastrointestinal, la enfermedad de Chagas afecta especialmente al colon y el esófago. La frecuencia con la que produce un compromiso digestivo varía entre el 5 y el 35%, que deriva en trastornos variados y dilataciones localizadas, como la esofágica, que cursa con disfagia (dificultad para tragar).
Los pacientes con afectación colónica secundaria a la enfermedad de Chagas padecen de estreñimiento progresivo, producto de una dilatación colónica o megacolon.
La enfermedad de Chagas se confirma a través de análisis de laboratorio, como son la visualización directa del parásito en sangre durante la fase aguda o a través de detección en el suero de anticuerpos específicos contra el parásito (diagnóstico serológicos), que se evidencian en la fase crónica de la enfermedad.
Tratamiento
El tratamiento de la enfermedad de Chagas continúa utilizando dos fármacos desarrollados hace más de 40 años: el benznidazol y el nifurtimox, que varían ampliamente en su tasa de curación, según la fase de la enfermedad.
Pesa a su relativa toxicidad- que le impide ser empleado durante el embarazo y produce reacciones adversas- el benznidazol se considera el estándar de tratamiento en la actualidad.
Prevención
- Detección del parásito en recién nacidos de madres provenientes de zonas endémicas, ya que el tratamiento temprano es la estrategia más efectiva.
- Diagnóstico de la infección en las mujeres en edad fértil procedentes de áreas endémicas para frenar la transmisión vertical en los embarazos y aplicar el tratamiento oportunamente.
- El control de los insectos vectores sigue siendo el mejor método de prevención, pero los insecticidas químicos tradicionales sólo sirven para combatir los vectores domiciliarios, pero últimamente se ha reportado resistencia a algunos de ellos. Para en el caso de los extra domiciliarios, no existe un producto que sea efectivo.
Para subsanar este problema, la Universidad Nacional de México (UNAM) ha desarrollado un biofungicida eficaz contra la chinche besucona, que es responsable del 74% de los casos de enfermedad de Chagas. Además, esta fórmula- basada en el hongo Metarhizium anisopliae– es inocua para los seres humanos y otros organismos vivos, pero no causa daño ambiental, pero es capaz de eliminar del 88 a 92% de la chinche más abundante en México. El hongo tiene la capacidad de eliminar al vector en cualquiera de sus etapas: huevecillo, ninfa o adulto, por lo que pronto podrán registrar la marca.