Fármaco experimental salva paciente con coronavirus

La mujer evolucionó satisfactoriamente, después de haber estado en peligro de muerte. Fármaco experimental salva paciente con Coronavirus.
El pasado 26 de febrero, el Centro Médico Davis de la universidad de California, en Sacramento, obtuvo los resultados confirmatorios de las pruebas de ARN para SARS-CoV-2 en una paciente, tras tratarla durante una semana con remdesivir por padecer COVID-19. La mujer evolucionó satisfactoriamente, después de haber estado en peligro de muerte.
Dentro de las terapias empleadas de manera experimental para el COVID-19 se encuentra el antiguo antipalúdico Cloroquina, el mensajero inmunitario antiviral Interferón y Kaletra (lopinavir y ritonavir), que corresponde a la combinación de dos inhibidores de la proteasa, utilizados para tratar la infección por VIH. También se administra el remdesivir, en casos de uso compasivo para esta infección, con pacientes graves.
Con la mayoría de los medicamentos en investigación, que han sido probados en monos macacos, se ha visto que existe una buena correlación entre la administración del medicamento y una disminución de la viremia.
La primera enferma de Estados Unidos
Recientemente se conoció el caso de una mujer, que fue detectada como el primer caso probable de propagación de COVID-19 en la comunidad estadounidense, de la que se desconocía la fuente de su infección: no había viajado fuera de los Estados Unidos a un área infectada ni había estado en contacto con un caso confirmado conocido.
Tuvieron que pasar 4 días antes de que los Centros para el Control y la Prevención de Enfermedades de EE. UU. (CDC) acordaran testear sus muestras. Esto se debió a que la mujer no cumplía con los estrictos criterios que la agencia tenía en ese momento, por lo que recién el 26 de febrero, el Centro Médico Davis obtuvo los resultados confirmatorios de la prueba de PCR que se le practicó a esta paciente.
Después de ese período de alerta y debido a su gravedad, los médicos de la institución sanitaria obtuvieron un permiso de uso compasivo por parte de la Administración de Alimentos y Medicamentos (FDA) para probar un fármaco experimental, fuera de un ensayo clínico. La droga testeada fue remdesivir, que es elaborada por la farmacéutica Gilead Sciences y se administra por vía intravenosa.
El antirretroviral
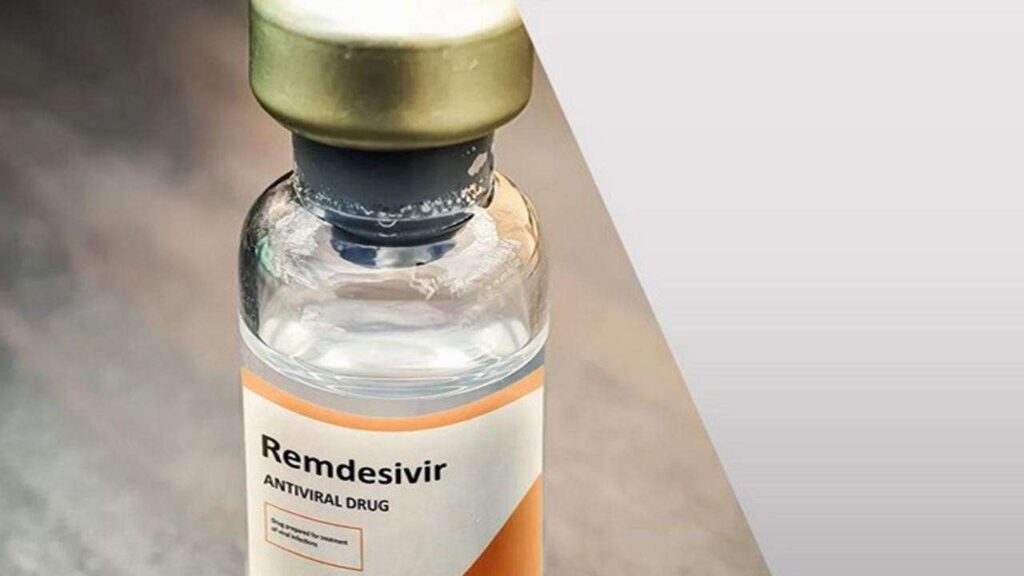
En cuanto a su mecanismo de acción, remdesivir no se dirige específicamente al SARS-CoV-2, sino que inhibe una enzima llamada ARN polimerasa, que es esencial para la polimerización del ARN viral, mecanismo que muchos virus usan para replicarse.
Se sabe que este medicamento resultó eficaz en ensayos in vitro y en estudios realizados en animales infectados con coronavirus humanos procedentes del SARS y del síndrome respiratorio del Medio Oriente, que causan cuadros respiratorios similares.
Varios ensayos aleatorizados y controlados con placebo para tratar el COVID-19 se están llevando a cabo con remdesivir, tanto en China como en los Estados Unidos, para verificar o para descartar su funcionamiento en pacientes.
En otro estudio, se usó este medicamento en tres pacientes con COVID-19, cuyos resultados se calificaron de “mixtos” al considerar las mejoras en cuanto a fiebre, requerimientos de oxígeno y resultados de carga viral. Estos resultados se compararon con los pacientes hospitalizados que no recibieron el fármaco.
Datos del especialista
George Thompson, un especialista en enfermedades infecciosas del Centro Médico Davis de la UC, que formó parte del equipo que atendía a la paciente, brindó una entrevista a Science Insider sobre el caso, la cual ha sido resumida para mayor comprensión de los lectores.
Thomson indicó que en el caso de la paciente, desde que se confirmó su diagnóstico hasta que se aplicó la terapia, pasaron unas 36 horas, que es un lapso de tiempo muy corto como para la aprobación de emergencia de un medicamento en investigación. Esto se debió a que creían que iba a fallecer.
Si bien se había hablado de emplear terapia de oxigenación con máquina extracorpórea (ECMO), no llegó a hacerse efectivo, pues se empezó a recuperar satisfactoriamente tras la medicación. Fármaco experimental salva paciente con Coronavirus.
Aunque se sabe que la precocidad en el empleo de los antirretrovirales es clave para los tratamientos de las virosis agudas, un requisito para administrar el remdesivir era que la paciente debía tener una prueba positiva de SARS-CoV-2, para así asegurarse de que no había eliminado el virus espontáneamente de su organismo.
Desde el día posterior a la infusión del fármaco, la paciente fue mejorando constantemente. Sin embargo, este resultado no pudo probar exactamente causa-efecto, debido a la imposibilidad de realizar la prueba de reacción de polimerasa en cadena (PCR) en su sangre. Esto se debió a la falta de recursos del sistema de salud; además, la paciente ya tenía una infección confirmada y no era una prioridad para usar en ella esta cara determinación.
Pero próximamente se va a poder realizar la PCR que fue aplazada, pues las muestras de la paciente están guardadas en el hospital local. El hecho es que dicho fármaco experimental salva paciente con Coronavirus.
¿Menor carga viral?
Si la disminución en sus cargas virales está temporalmente relacionada con remdesivir, especialmente dentro de las 24 horas, es un argumento mucho más convincente del funcionamiento del fármaco. Aunque se ha sabido que muchos pacientes con COVID-19 solo tienen el virus en sus muestras respiratorias, sin viremia asociada.
Dadas las escasas experiencias con el fármaco, que quedaría reservado para usarse precozmente en las enfermedades infecciosas de mayor gravedad, debe ser evaluado en relación con el riesgo versus el beneficio, pues puede causar una severa hepatotoxicidad.
El centro médico ha sido contactado por varias compañías para probar diferentes drogas experimentales en ensayos clínicos. Existe mucho interés en testear la cloroquina y el interferón con Kaletra, ya que aún queda mucho por aprender. El tiempo apremia y no existe vacuna ni tratamiento opcional que resulte comprobadamente eficaz.
Para leer la nota original, pulsar aquí.