Emplean terapia de fagos en adolescente con fibrosis quística

El complejo Mycobacterium abscessus incluye un grupo de micobacterias no tuberculosas de rápido crecimiento y que muestran multirresistencia a los antibióticos. Además es resistente a los desinfectantes, por lo que puede ocasionar infecciones posquirúrgicas y después de realizar procedimientos diagnósticos y terapéuticos diversos.
Son responsables de enfermedades de variada ubicación: piel y tejidos blandos, infecciones del sistema nervioso central, infecciones oculares, bacteremia y otras. También, M. abscessus se han asociado con brotes ocurridos durante procedimientos de tipo cosméticos y en transmisiones hospitalarias.
M. abscessus y otras bacterias suelen colonizar la espesa mucosidad que se acumula en los pulmones de las personas que padecen fibrosis quística (FQ), una enfermedad genética que afecta a unas 80,000 personas en todo el mundo. Estas infecciones terminan ocasionando daños pulmonares graves, por lo que puede requerirse un trasplante pulmonar, como última alternativa.
Terapia con fagos
La terapia con fagos -virus que parasitan y destruyen bacterias- data de hace aproximadamente un siglo, pero esta idea medicinal fue restringida ámbito complementario, principalmente debido al uso de los antibióticos.
En comparación con los antibióticos de amplio espectro, los fagos son de tipo específico, pues matan a una sola cepa bacteriana, lo que significa que un tratamiento que es exitoso para tratar la infección de un paciente, puede fallar en otra, que posea una variante de la misma bacteria.
La terapia con fagos ha sido difícil de aprobar por los organismos sanitarios, dadas ciertas dudas en cuanto a su seguridad, por el hecho de que el virus tiene la capacidad de auto replicarse y evolucionar, e incluso se teme que pueda dotar de resistencia a bacterias que normalmente son inocuas.
Al igual que ocurre con la antibioticoterapia y otros tratamientos contra las enfermedades bacterianas, ciertas endotoxinas son liberadas por la bacteria al ser destruidas dentro del paciente, que puede ocasionar una serie de reacciones tóxicas de variada gravedad.
Pero basados en una serie de recientes éxitos en casos de bacterias resistentes a los antibióticos, ha resurgido el interés de importantes universidades norteamericanas por focalizarse en la investigación de fagos, donde algunas cepas de tuberculosis farmacorresistentes podrían constituir en un blanco potencial para este tipo de terapia.
Fagos experimentales: un caso clínico
La paciente de 15 años Isabelle Carnell- que padece de fibrosis quística– durante varios años había estado combatiendo sin éxito una infección multirresistente de M. abscessus, pues estaba agravándose a medida que transcurría el tiempo. Como resultado de este patógeno, Isabelle había perdido dos tercios de su función pulmonar y su infección persistía aún después del trasplante, poniendo en riesgo su vida.
Una semana después de recibir un doble trasplante de pulmón- en septiembre de 2017- la herida de la incisión quirúrgica se inflamó de manera importante, impidiendo su cicatrización.
Al fallar los tratamientos convencionales, la madre de Isabelle le preguntó a Helen Spenser, su pediatra del Hospital Great Ormond Street de Londres sobre alternativas, agregando que había leído sobre el uso de virus para matar bacterias (fagos), ante lo cual Spencer decidió arriesgarse y probar con esta terapia, para lo cual colaboró estrechamente con el grupo del experto en fagos Graham Hatfull de la University of Pittsburgh en Pennsylvania.
Hatfull y su equipo mantienen una de las colecciones de bacteriófagos más grandes del mundo, consistente en más de 15,000 de estos virus, entre los cuales encontraron 3 fagos con el potencial de lisar a M. abscessus aislado de las heridas y el esputo de Isabelle, después de haber tardado 3 meses en encontrarlos. El grupo de Hatfull combinó los tres fagos para reducir las posibilidades de que M. abscessus desarrollara resistencia.
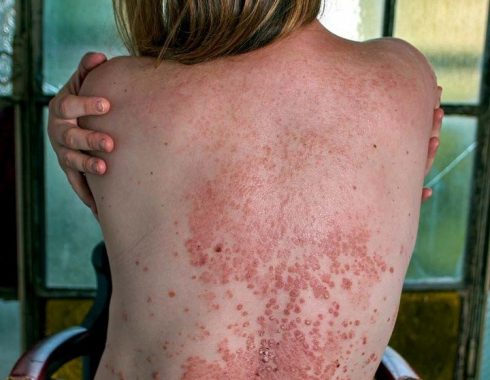
Isabelle recibió su primera infusión de fagos en junio de 2018. Después de 72 horas, sus heridas empezaron a curarse. Al completar 6 semanas de tratamiento intravenoso cada 12 horas, la infección había desaparecido. Después de 6 meses de la terapia de fagos- que fue bien tolerada- se evidenció una mejoría clínica, que incluyó el cierre de la herida esternal post quirúrgica, mejoró la función hepática y los nódulos cutáneos infectados, según informan los autores en Nature Medicine.
Actualmente recibe infusiones dos veces al día y también aplica el tratamiento en forma directa a las lesiones que aún restan, pues como manifiesta Spenser: «Somos optimistas de que con el tiempo puede eliminar completamente la infección«, si bien Isabelle lleva una vida adolescente más normal, realizando actividades propias de su edad, en compañía de sus amistades.
Expectativas y limitaciones
Spencer, Hatfull y sus coautores aclaran que Isabelle podría haber llegado a mejorar sin usar la terapia con fagos. También evidenciaron que su preparado de fagos diseñados a medida no es efectivo contra otras cepas aisladas de M. abscessus que han testeado.
Pese a este inconveniente, el éxito aparente ha motivado a los investigadores del área, como los pertenecientes a la colección de Hatfull a infectar y lisar cepas de a M. tuberculosis in vitro, que podrían ser útiles contra aquellas cepas bacterianas resistentes a los antibióticos y bacteriostáticos empleados en la actualidad.
Pero William Jacobs, un especialista en tuberculosis del Albert Einstein College of Medicine en la ciudad de Nueva York, ha probado esos fagos en un modelo de ratón con tuberculosis (TB) y no ha evidenciado mejoras, pues indica: «La TB vive dentro de las células y no creo que los fagos puedan entrar«, dice Jacobs (en comparación con M. abscessus que vive principalmente fuera de las células). Pero otros investigadores dicen que podría haber formas de transportar fagos al interior de las células infectadas.
Las compañías dedicadas a la investigación y desarrollo de terapias de fagos tienen al menos tres ensayos en curso para evaluar el valor potencial de sus productos para tratar varias infecciones bacterianas diferentes.
Pero en palabras de Madhukar Pai, epidemiólogo de la McGill University en Montreal, Canadá, que aún si estas terapias resultan exitosas, enfrentan grandes obstáculos prácticos y de índole económico: «Para que esto se convierta en una terapia del mundo real, necesitamos averiguar si podemos hacerlo con menos esfuerzo y costo«.