Virus que infecta a cerdos podría ayudar a destruir el cáncer
En los últimos 2 años, dentro de los tratamientos del cáncer, se ha reconocido como el avance del año a la inmunoterapia, como es el caso de la terapia de células T con receptores de antígenos quiméricos (chimeric antigen receptor, CAR), que ha llegado a ser considerada como un cambio innovador en la forma en que se trata el cáncer en los pacientes. Pero pese a lo esperanzador de sus resultados, no tardó en aparecer un caso de leucemia resistente a este tratamiento.
Pero como esta investigación sigue en la búsqueda de nuevas alternativas terapéuticas, la viroterapia aparece como un prometedor tratamiento, que hace uso de virus oncolíticos, que infectan y destruyen las células cancerosas de manera específica. Estos virus oncolíticos tienen características únicas que los diferencian de cualquier otro tratamiento anticancerígeno: dentro de las ventajas de la viroterapia se encuentra la falta de resistencia cruzada con otras terapias y la capacidad de destruir el tumor mediante una variedad de mecanismos que matan de manera selectiva a las células tumorales.
Un virus “bueno”
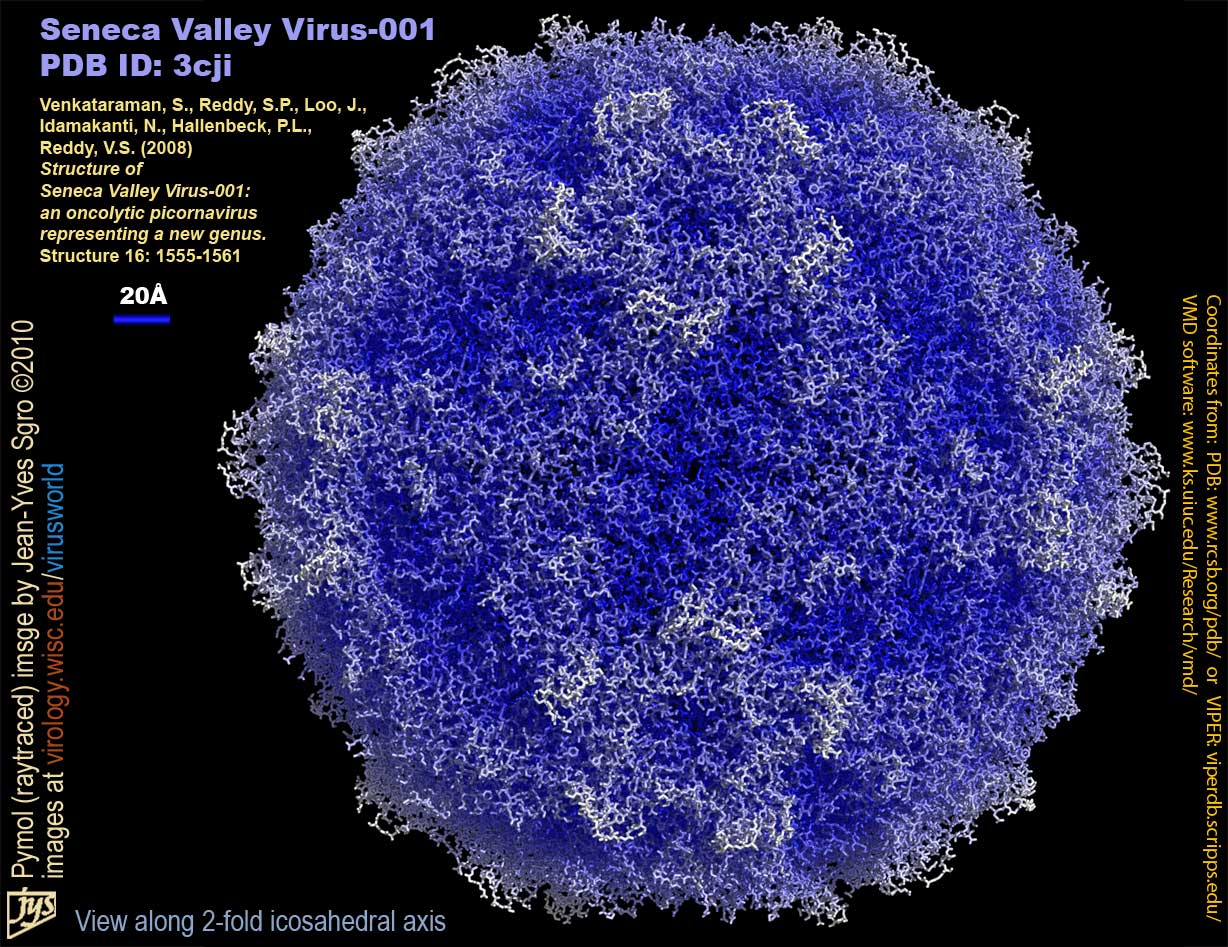
Virus de valle de Séneca en microfotografía electrónica.
El recientemente descubierto virus del valle de Séneca (VVS) -perteneciente a la familia de los picornavirus, que causa variadas infecciones en cerdos- resulta ser un virus oncolítico, que se encuentra dentro de los candidatos a convertirse en una innovadora forma de luchar contra el cáncer.
El comprender la estructura de estas partículas víricas es necesario para crear un virus efectivo que pueda producir la lisis de las células cancerosas, de forma tal que puedan ser usadas para desarrollar nuevas terapias efectivas con el menor riesgo posible para los pacientes. Esta necesidad llevó a un grupo de investigadores del Okinawa Institute of Science and Technology Graduate University (OIST) en Japón y de la University of Otago en Dunedin, Nueva Zelanda, a trabajar en un estudio publicado en Proceedings of the National Academy of Sciences, donde explican cómo el SVV interactúa con las células tumorales, sin dañar las células sanas.
Para examinar el mecanismo de acción del virus, los científicos utilizaron la microscopía crioelectrónica para capturar imágenes de miles de ellos, logrando visualizar su estructura en alta resolución. Descubrieron que el VVS tiene una propiedad inusual, porque se dirige a un receptor específico que se encuentra en las células tumorales, el ántraxreceptor de toxina 1 (ANTXR1). Por su parte, un receptor emparentado con éste, llamado ANTXR2, solo se expresa en tejidos sanos.
El hecho que el VVS se una de manera específica al receptor ANTXR1 -que está presente en las células tumorales de más del 60% de los cánceres humanos- podría convertirlo en una terapia adecuada para muchos tipos de cáncer, como explica el coautor del estudio, el profesor Matthias Wolf:
«Las diferencias entre los dos receptores son sutiles, pero, no obstante, estas diferencias sutiles hacen que uno se una al virus con alta afinidad, mientras que el otro no«. «Los componentes deben encajar como una llave en una cerradura; este es un sistema altamente evolucionado donde todo encaja perfectamente«.
Cómo evadir al sistema inmunológico
Los investigadores han empleado el VVS de manera exitosa en ensayos clínicos de fase temprana en tumores sólidos pediátricos y cáncer de pulmón de células pequeñas.
Aunque no existe una inmunidad innata ante este virus, pues no es un patógeno humano, el sistema inmunológico está normalmente programado para combatir los virus que son percibidos como una amenaza, por lo que son destruidos en un lapso de 2-3 semanas post infusión.
Para evadir los mecanismos inmunes, los investigadores analizan la estructura de VVS y encontrar maneras que permitan que el virus se replique y mate las células cancerosas durante un mayor tiempo, por lo que existe un creciente interés en la obtención de VVS mutantes, que puedan conservar su capacidad para unirse e infectar células tumorales y a la vez sean capaces de evitar la respuesta inmune antiviral del huésped, como explica la coautora autora principal del estudio, Prof. Mihnea Bostina:
«Podemos saber qué parte del virus es esencial para unirse al receptor y cuál no. Podemos tratar de cambiar las partes no esenciales para escapar de la acción del sistema inmunológico, mientras dejamos la parte esencial intacta».
Aunque los científicos continúan buscando una forma efectiva de evadir el sistema inmunológico, el equipo de investigadores cree que es posible modificar al VVS para que pueda reconocer diferentes receptores celulares, lo que lo convertiría en una excelente herramienta en la emergente viroterapia, para ser útil contra diferentes tipos de cáncer.
Otra alternativa para evitar la eliminación del virus del huésped humano sería realizar estudios que analicen las interacciones entre el VVS y los anticuerpos neutralizantes, para así identificar los residuos clave que se encuentran en la superficie de la cápside y que son responsables de la respuesta inmune y así poder evadirla.
Por su parte, el primer autor del estudio, Nadishka Jayawardena -estudiante graduado de la University of Otago- cree que esta investigación dará como resultado tratamientos altamente efectivos y específicos contra diversos tipos de cáncer.






